前言 单细胞三代测序揭示植物静止中心的发育轨迹,发表于2026年2月 本研究通过优化稀有细胞分离流程,结合单细胞三代全长RNA测序,首次系统绘制了拟南芥根尖静止中心(QC) 的转录组图谱,揭示了其在发育过程中从激素信号向分化转变的轨迹,发现并验证了新的QC标记基因 RGF10 与关键调控因子 TEL1,并通过跨物种比较揭示了水稻与拟南芥QC在生长素通路上的进化差异。

研究背景
植物的根尖干细胞微环境由静止中心(QC) 及其周围的初始细胞构成,QC通过分泌信号维持干细胞的未分化状态,其功能异常将导致根发育停滞。然而,QC细胞数量稀少,传统单细胞测序难以获得高质量、全长度的转录组信息。本研究开发了一种高效分离QC细胞的方法,并利用单细胞三代全长RNA测序SCAN-seq技术,实现了对QC细胞的全长转录组解析,为理解植物干细胞维持机制提供了前所未有的视角。
技术路线
研究发现
稀有细胞高效分离与转录本新发现 图1. SCAN-seq技术能高效捕获QC细胞,并首次揭示QC中存在大量未知转录本与复杂剪接事件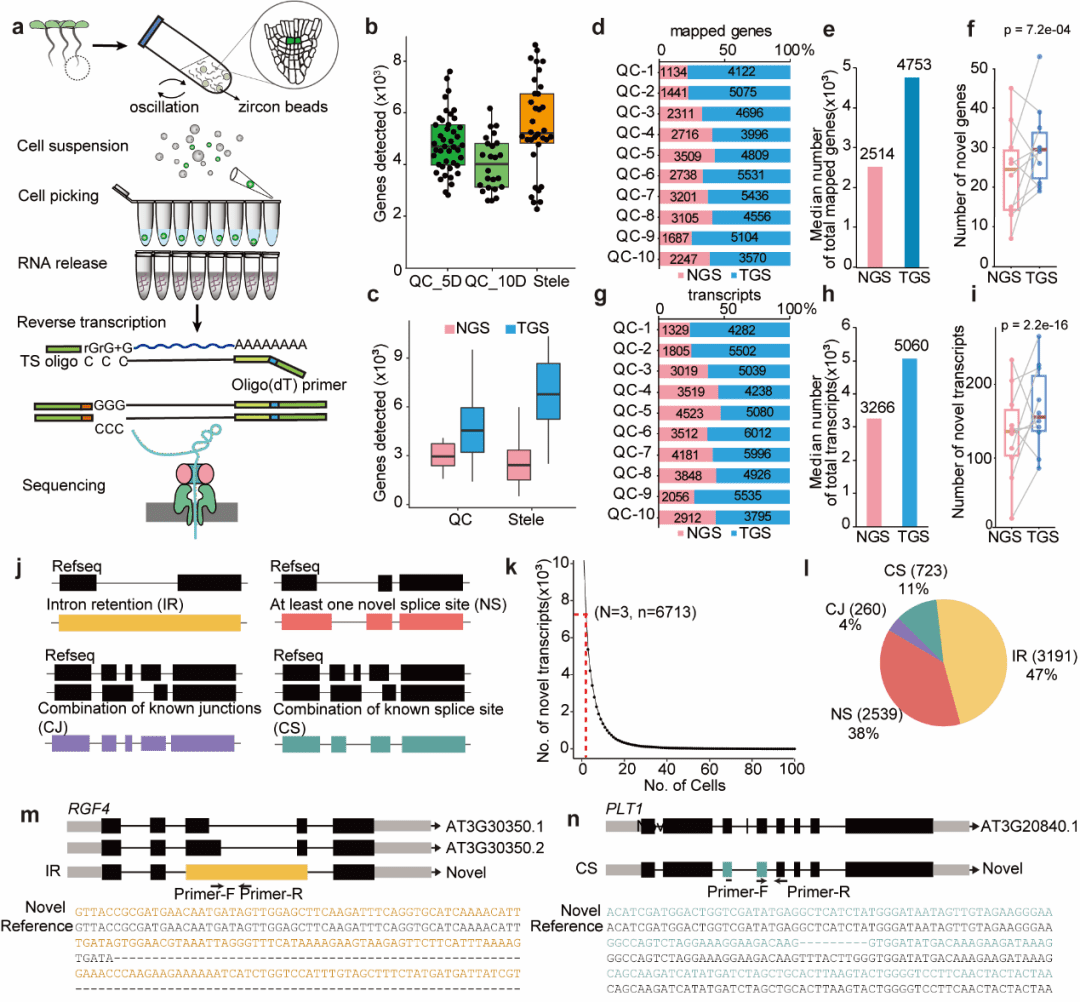
研究团队利用拟南芥pWOX5::GFP(QC标记)和pSHR::GFP(中柱标记)转基因系,通过优化酶解步骤(添加锆珠、提高振荡速度),将QC细胞得率提升至0.5%(传统方法仅为0.063%)。随后对单个GFP阳性细胞进行(基于Nanopore平台)。 发现: ● 检测效率提升:SCAN-seq在单个QC细胞中平均检测到4,822个基因,显著高于10x Genomics平台(图1c)。 ● 新转录本爆发:共鉴定出6,713个未注释转录本,其中内含子保留(IR)类型占比最高(47%),提示QC存在广泛的可变剪接调控(图1j–l)。 ● 验证新转录本:通过RT-PCR和Sanger测序,证实了PLT1和RGF4存在新的剪接异构体,并发现这些异构体可能通过改变蛋白结构或触发无义介导的降解(NMD)来调控QC功能(图1m–n)。
QC特异性标记基因的鉴定与验证 图2. RGF10和TEL1是QC新的特异性标记基因,可作为QC功能研究的重要工具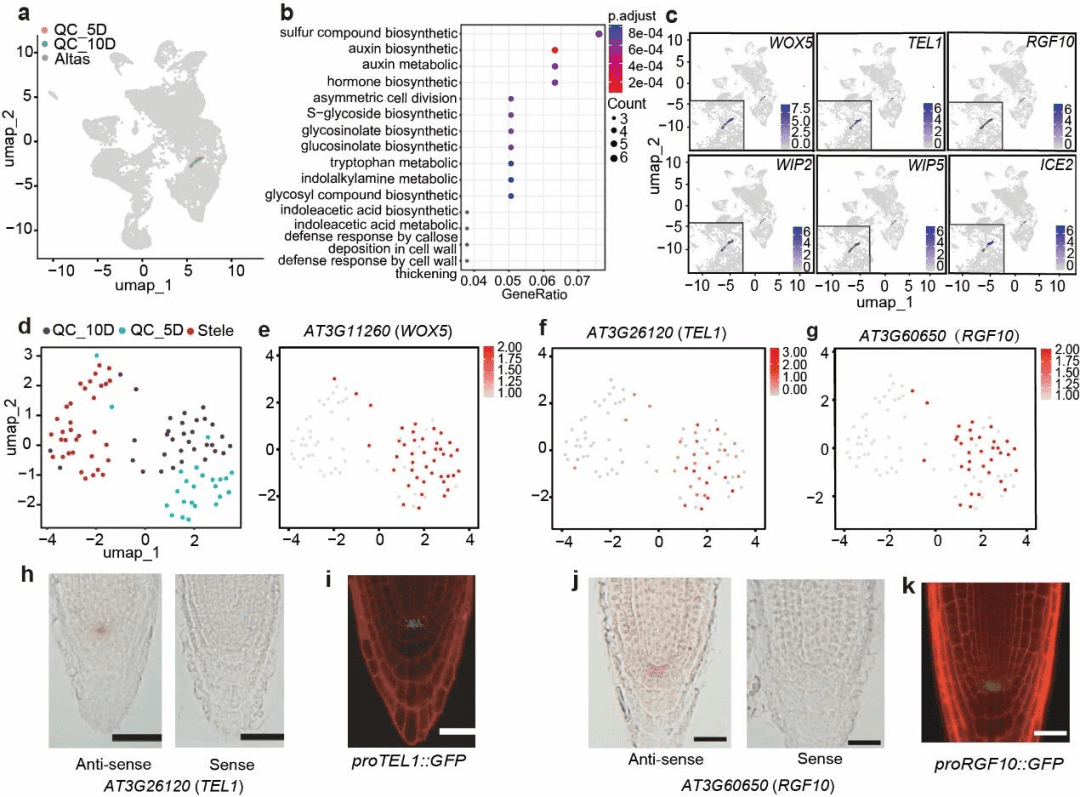
将单细胞三代全长RNA测序数据与已发表的拟南芥根单细胞图谱整合(UMAP聚类),筛选QC富集基因,并通过原位杂交和转基因报告株系进行验证。 发现: ● 已知标记验证:WOX5被确认为QC最显著上调基因,验证了数据可靠性。 ● 新标记发现: ○ RGF10和TEL1被鉴定为QC特异性基因,其表达在QC细胞中高度富集(图2f–g)。 ○ 通过RNA原位杂交和proTEL1::GFP、proRGF10::GFP报告株系,证实两者仅在QC区域表达(图2h–k)。 ● 功能提示:GO分析显示QC富集基因显著参与“生长素合成”通路(图2b),与QC的干细胞调控功能一致。
QC从增殖向分化的转录组转变 图3. QC在发育过程中经历从“干细胞维持”向“分化支持”的转录组重编程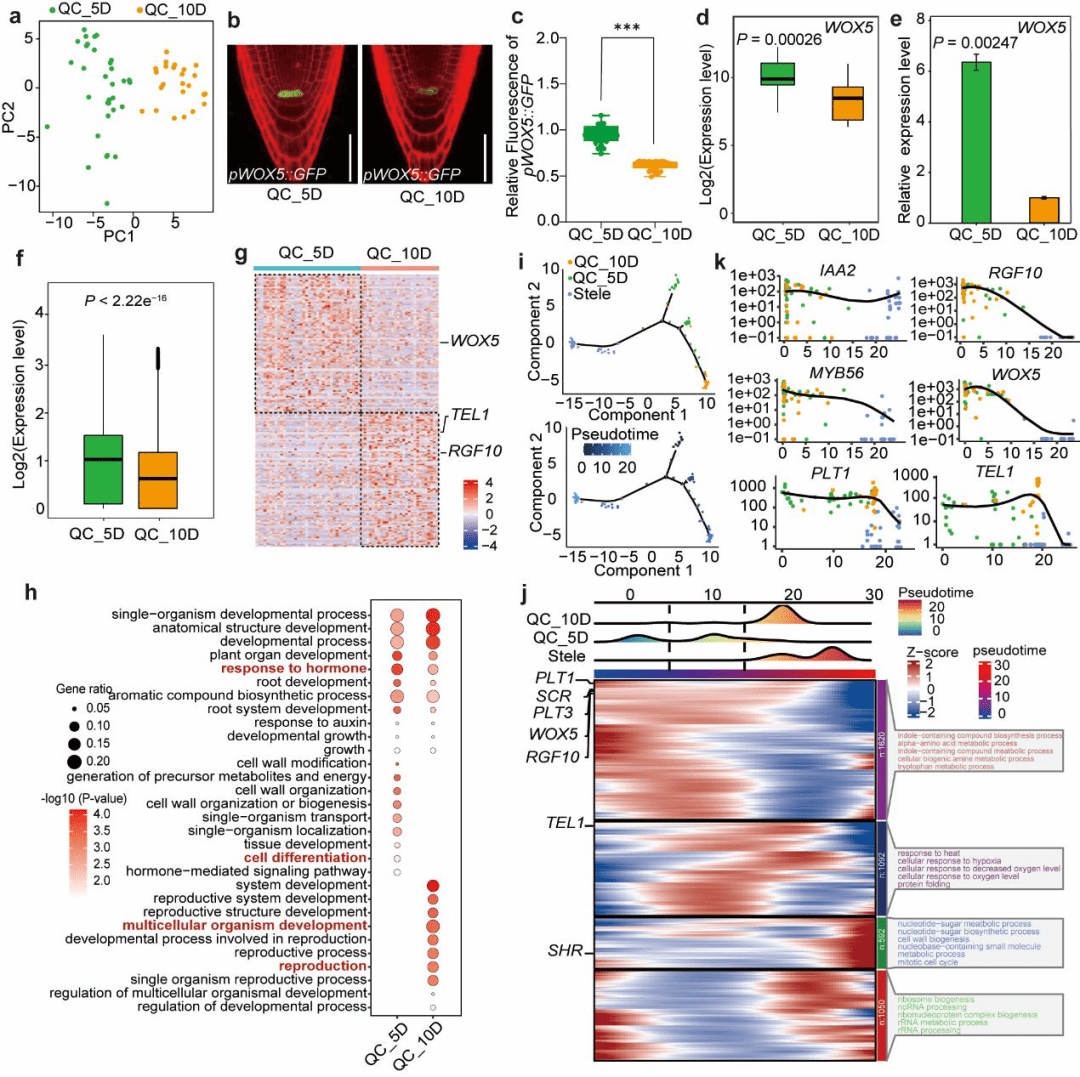
比较5天(QC_5D) 与10天(QC_10D) 的QC细胞转录组,结合拟时序分析(Monocle2),追踪QC发育轨迹。 发现: ● 发育阶段差异: ○ QC_5D高表达细胞周期、生长素响应基因;QC_10D则高表达与根分化相关的基因(图3g–h)。 ○ WOX5表达在QC_5D中显著更高,与pWOX5::GFP荧光强度下降趋势一致(图3b–e)。 ● 拟时序轨迹: ○ 从QC_5D → QC_10D → 中柱细胞,呈现出从“激素合成与细胞分裂”向“细胞壁合成与根发育” 的功能转变(图3i–k)。 ○ 关键基因如IAA2(生长素诱导)在早期高表达,而PLT1(分化相关)在后期上升。
TEL1通过抑制WOX5维持QC结构 图4.TEL1是QC静止状态的关键维持因子,其缺失导致WOX5过表达、细胞周期异常启动和QC结构破坏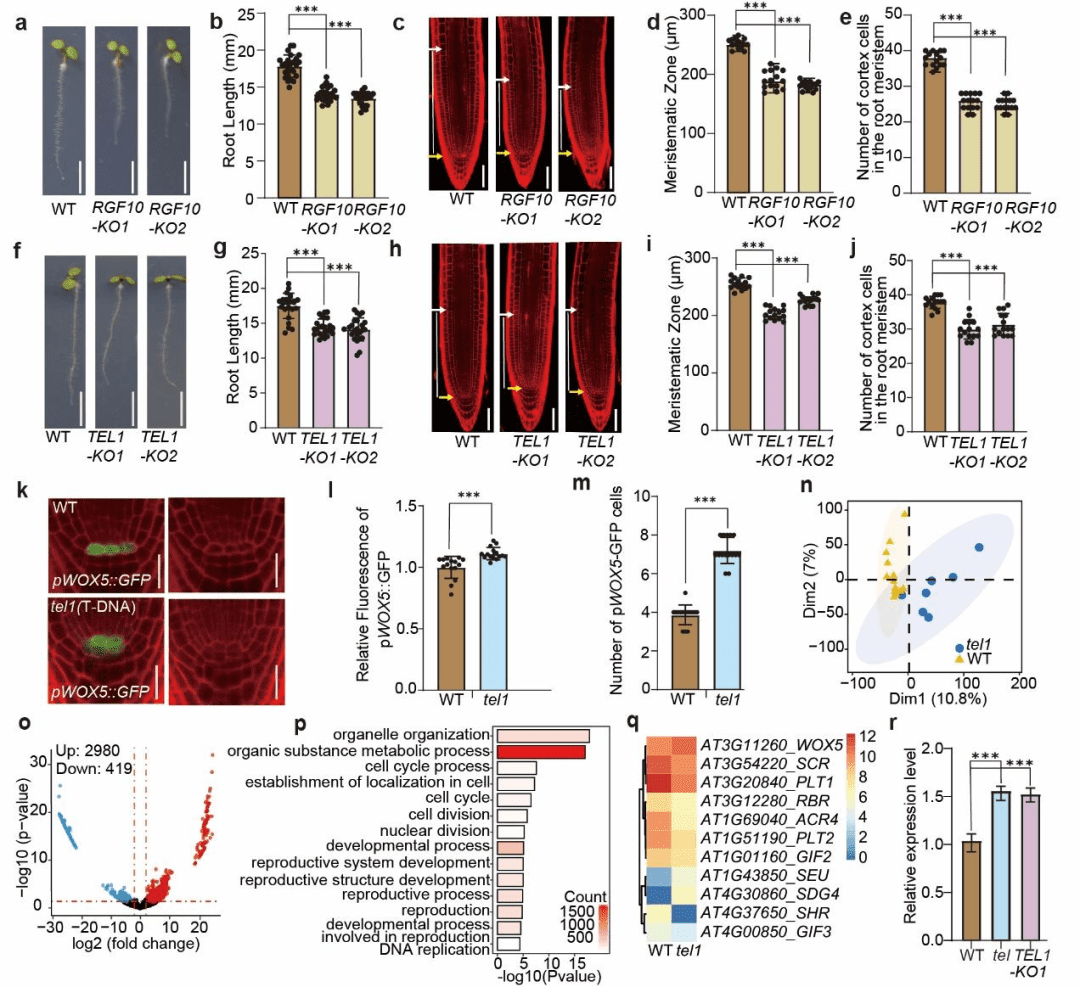
利用CRISPR-Cas9构建RGF10和TEL1敲除株系,结合细胞学观察、单细胞RNA-seq(SMART-seq2)和RT-qPCR,解析其功能。 发现: ● RGF10功能: ○ 敲除后主根变短、分生组织变小(图4a–e),但QC形态正常,提示RGF10主要调控根生长而非QC结构。 ● TEL1功能: ○ 敲除导致主根缩短、分生组织减小,QC结构紊乱、细胞数量增加(图4f–k)。 ○ pWOX5::GFP荧光强度和WOX5表达显著升高(图4l–r),表明TEL1负调控WOX5。 ○ 单细胞转录组分析显示,TEL1敲除后,细胞周期相关基因(如Cyclin、WEE1)上调,证实TEL1通过抑制细胞周期维持QC的“静止”状态(图4o–p)。
水稻与拟南芥QC的进化差异 图5. 单子叶与双子叶植物QC在转录组结构和激素调控网络上存在明显分化,为作物根系改良提供了重要线索 构建水稻pOsQHB::GFPQC标记系,分离水稻QC细胞进行SCAN-seq,与拟南芥QC转录组进行比较分析。 发现: ● 表达谱差异: ○ 水稻QC中低表达基因比例更高,整体转录活性低于拟南芥(图5c–d)。 ● 同源基因表达模式: ○ 共鉴定出7,644个共同表达基因,但存在物种特异性基因(拟南芥788个,水稻751个)(图5j)。 ○ 水稻特异性基因富集于“细胞稳态”“寡糖代谢”等通路;拟南芥特异性基因富集于“受体激酶信号”等通路(图5k)。 ● 生长素通路分化: ○ 拟南芥QC高表达IAA30、LAX2等,而水稻QC高表达IAA16、IAA13、AUX2/11等(图5l),提示两者在生长素信号转导策略上存在显著进化差异。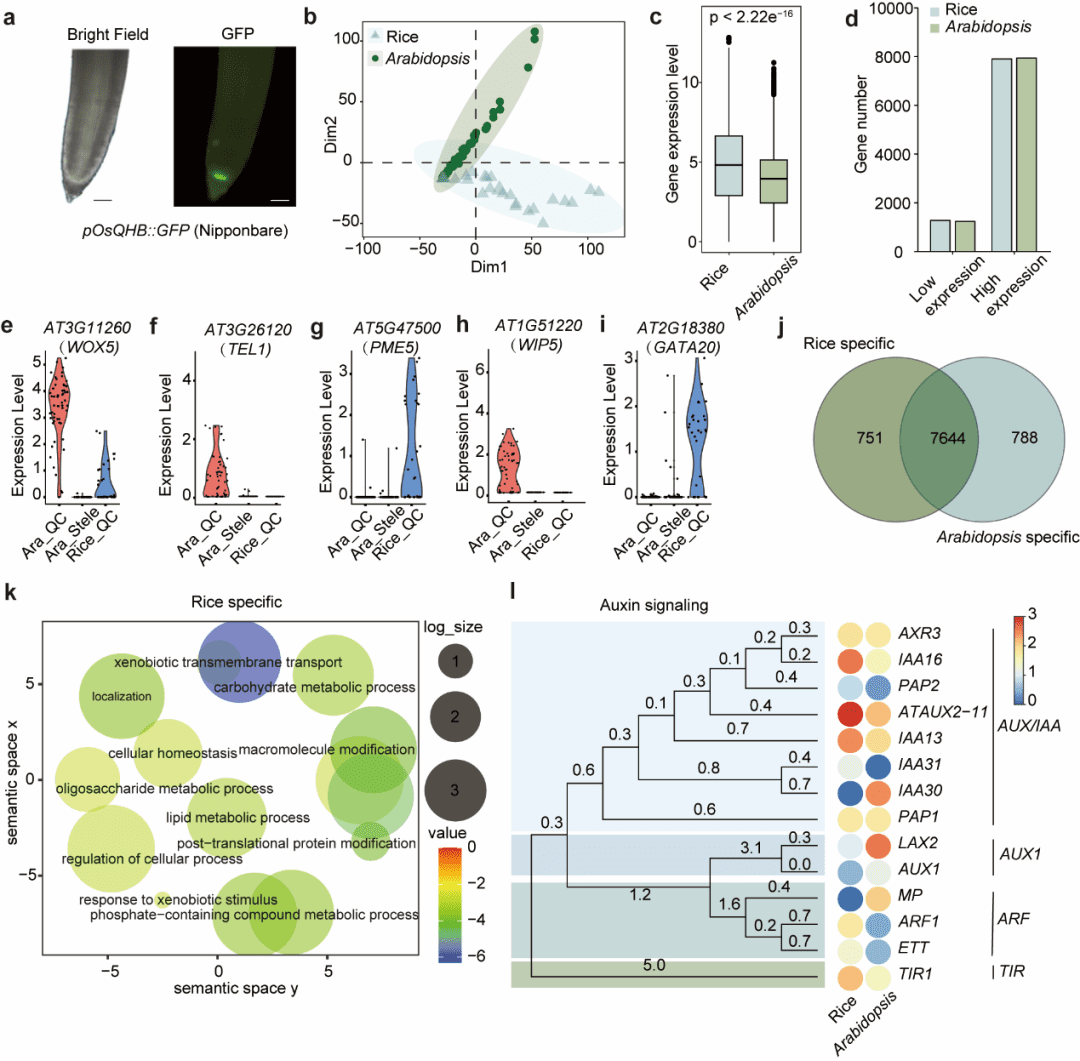
研究总结
本研究通过技术创新(高效QC分离 + 三代单细胞测序) 与深入功能验证,在多个层面推动了植物干细胞研究: 1. 技术突破:建立了适用于稀有植物细胞类型的单细胞全长转录组分析流程,显著提高基因检测灵敏度与新转录本发现能力。 2. 资源贡献:构建了拟南芥QC在关键发育阶段的转录组图谱,并首次发布水稻QC单细胞数据,为跨物种比较提供了高质量资源。 3. 机制新认知: ○ 鉴定RGF10为QC功能相关的新标记基因。 ○ 揭示TEL1通过抑制WOX5及细胞周期基因,维持QC静止状态的机制。 ○ 发现QC发育过程中存在从“增殖”到“分化”的转录组重编程。 4. 进化视角:首次系统比较单子叶与双子叶植物QC的转录组差异,为理解根干细胞调控的保守性与多样性提供了关键数据。 该研究不仅深化了对根尖干细胞维持机制的理解,也为通过调控QC活性改善作物根系结构提供了新的靶点和思路。
参考文献 Hu, G., Li, C., Guo, W., Li, D., Yang, L., & Gu, X. (2026). Single-cell transcriptomic analysis of plant quiescent center by third-generation sequencing reveals developmental trajectories. Genome Biology. https://doi.org/10.1186/s13059-026-03989-0
推荐阅读
解锁植物时空奥秘 | 空间转录组Stereo-seq助力您的研究更进一步
