单细胞RNA测序显示,参白解毒通过调控免疫抑制树突状细胞的 TMEM131-TNF 信号通路介导分化,延缓结直肠肿瘤发生
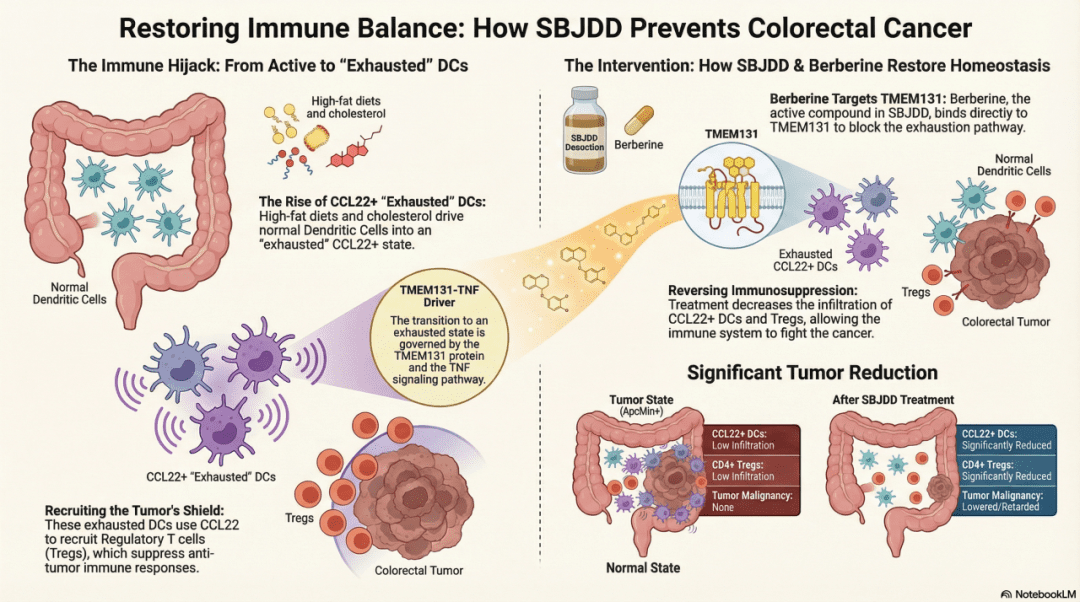
本研究利用单细胞RNA测序技术,首次揭示中药复方参白解毒方(SBJDD) 通过调控TMEM131-TNF信号通路,抑制CCL22⁺免疫抑制性树突状细胞的分化与功能,从而有效延缓结直肠肿瘤发生,其活性成分小檗碱是关键效应分子。
研究背景
结直肠癌是我国高发的恶性肿瘤之一,其发生发展与肿瘤微环境密切相关。近年来,免疫细胞在肿瘤发生中的作用备受关注,其中树突状细胞作为抗原提呈的核心细胞,既可激活抗肿瘤免疫,也可能在特定条件下转化为免疫抑制性亚群,促进肿瘤免疫逃逸。
参白解毒方(SBJDD)是一种临床用于结直肠腺瘤防治的中药复方,前期研究已证实其具有降低腺瘤复发率的作用。然而,SBJDD如何重塑肿瘤微环境、调控免疫细胞功能,其具体机制尚不明确。
本研究通过单细胞转录组学,系统描绘了SBJDD干预下结直肠肿瘤微环境的细胞图谱,揭示了其关键靶点与信号通路,为中药复方的现代化研究提供了新范式。
技术路线
1. 动物模型:使用ApcMin/+自发性结直肠癌小鼠,给予高脂饮食诱导肿瘤发生,同时灌胃SBJDD。
2. 临床验证:收集多发性结直肠腺瘤患者服用SBJDD前后的组织样本。
3. 单细胞测序:对小鼠和临床样本进行10x Genomics单细胞RNA测序,构建肿瘤微环境细胞图谱。
4. 细胞互作与轨迹分析:利用CellChat、拟时序分析等手段,揭示细胞分化轨迹与免疫细胞间相互作用。
5. 机制验证:通过基因敲低、分子对接、表面等离子体共振等方法,鉴定关键靶点与活性成分。
6. 成分分析:采用UHPLC-QTOF-MS鉴定SBJDD入血成分,筛选关键活性分子。
研究发现
01
SBJDD抑制结直肠肿瘤发生与CNV水平
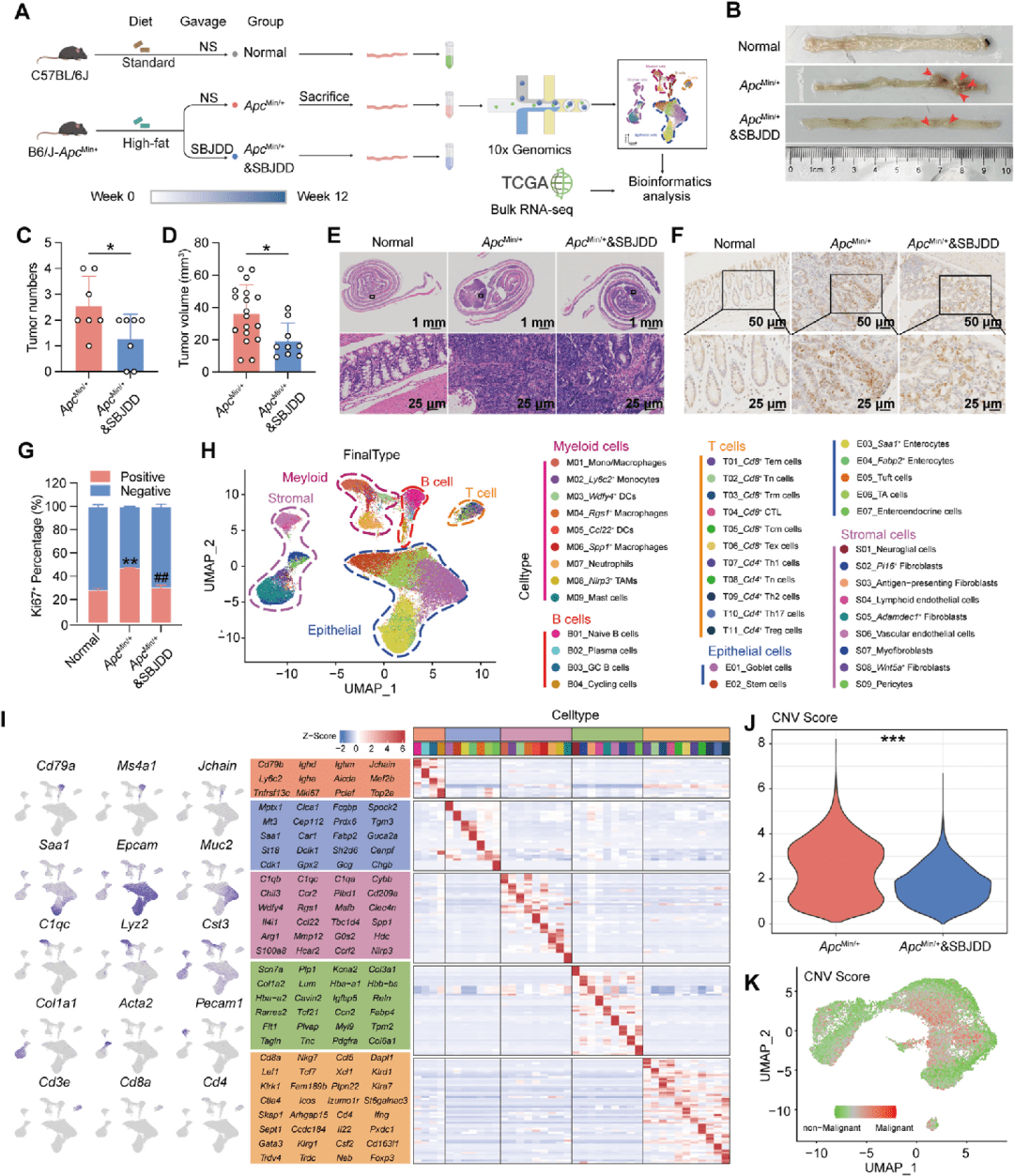
建立 ApcMin/+ 自发性结直肠癌小鼠模型(n=7/组),给予高脂饮食,SBJDD灌胃干预12周。通过H&E染色、Ki67免疫组化评估肿瘤负荷与增殖活性。对48,992个单细胞进行10x Genomics单细胞RNA测序(样本来源:正常组、ApcMin/+模型组、SBJDD治疗组小鼠结直肠组织)。利用InferCNV推断上皮细胞拷贝数变异。
具体发现:
● SBJDD显著减少肿瘤数量(从模型组的平均15.2个降至4.3个)、体积与恶性程度
● Ki67阳性细胞比例从模型组的42.7%降至18.3%
● 单细胞UMAP聚类显示5大细胞类型(上皮细胞、基质细胞、髓系细胞、B细胞、T细胞)及40个细胞亚型
● 上皮细胞CNV评分:模型组显著高于正常组,SBJDD治疗组显著降低
02
Ccl22+ DCs在肿瘤微环境中显著富集
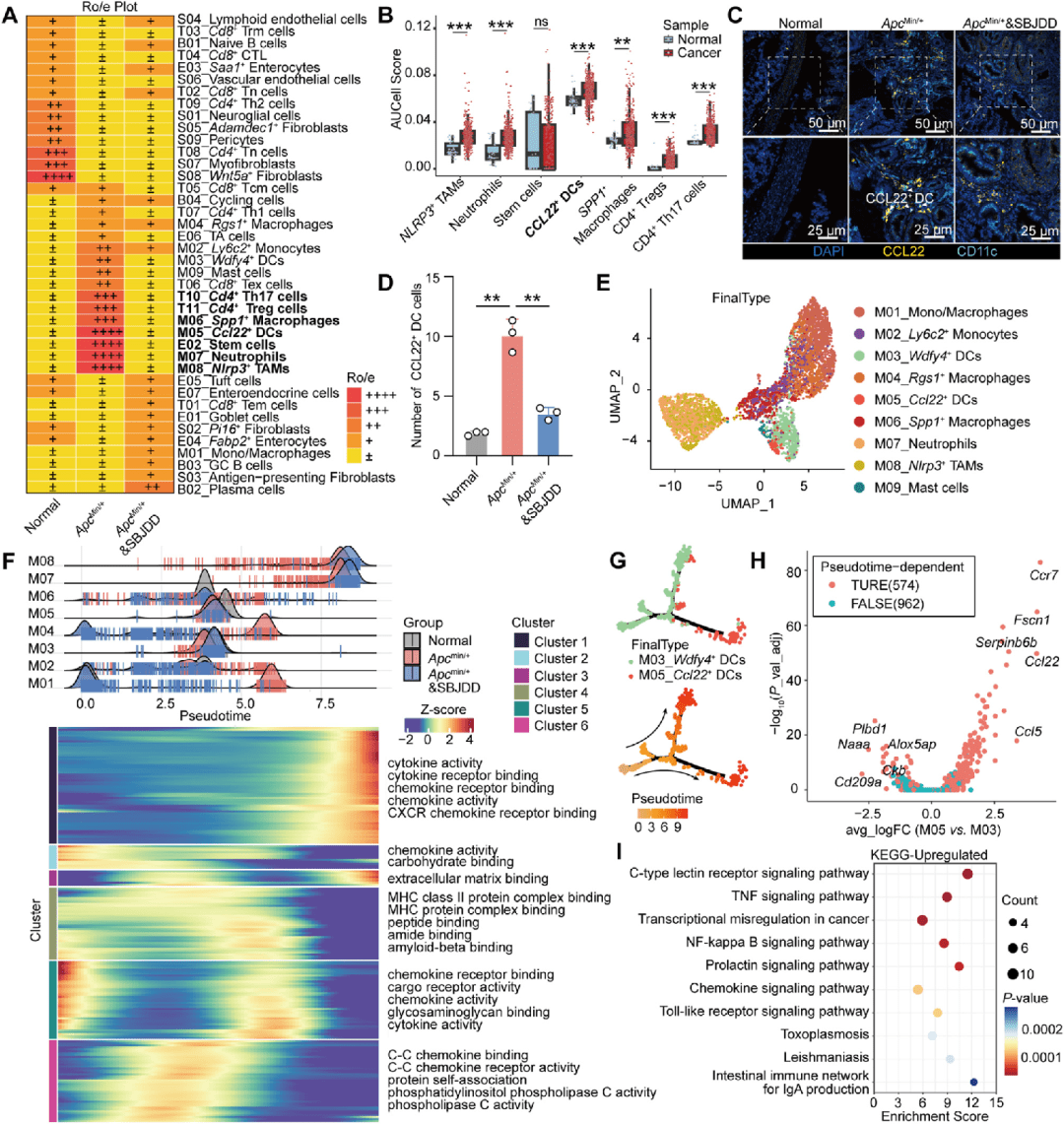
对上述48,992个单细胞数据进行细胞亚群丰度分析(Ro/e比值),结合TCGA-COAD数据库计算AUCell评分。利用mIHC多重免疫组化(样本:小鼠结直肠组织切片)验证细胞浸润。采用Monocle2进行拟时序分析,追踪髓系细胞分化轨迹。
具体发现:
● Ro/e分析显示 Ccl22+ DCs在模型组显著富集(Ro/e > 2),SBJDD治疗后富集程度降低
● TCGA数据库中 CCL22+DCs在CRC组织中AUCell评分显著高于正常组织
● mIHC证实:模型组 CCL22+ DCs密度为正常组的4.2倍,SBJDD治疗后下降至1.8倍
● 拟时序分析揭示 Ccl22+DCs来源于 Wdfy4+ DCs,位于分化轨迹末端,伴随TNF信号通路相关基因上调
03
Ccl22+ DCs与Treg细胞形成免疫抑制网络
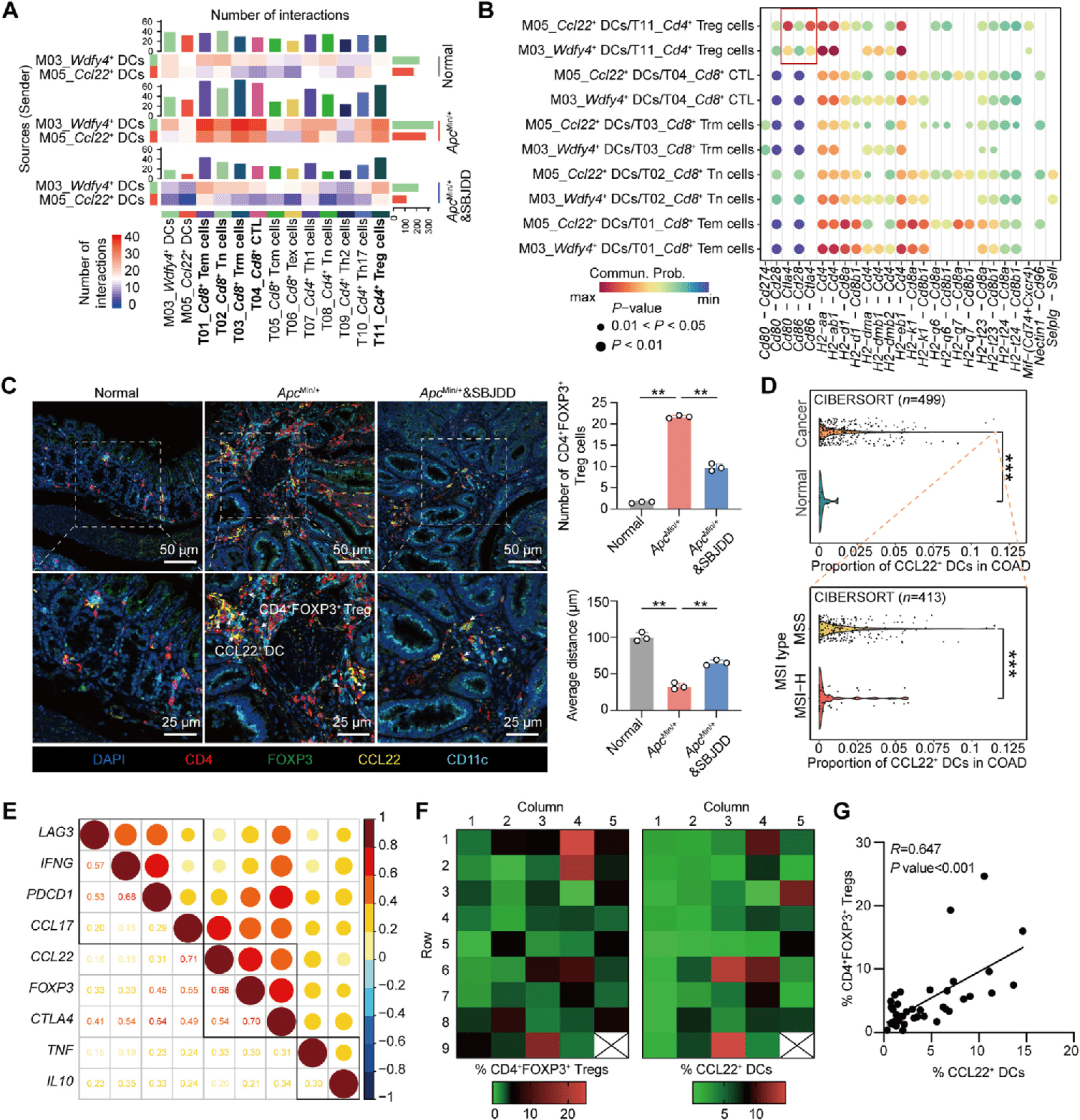
使用CellChat进行细胞间配体-受体互作分析(基于小鼠scRNA-seq数据)。mIHC共定位分析检测 CCL22+ DCs与 CD4+FOXP3+ Tregs的空间距离。基于TCGA数据库进行相关性分析。组织微阵列(TMA,样本:90例结直肠癌患者组织)验证细胞丰度相关性。
具体发现:
● CellChat显示 Ccl22+DCs与 CD4+ Tregs之间互作强度在模型组显著增强,主要介导分子为 CD80/CD86–CTLA4
● mIHC证实:模型组中 CCL22+ DCs与Tregs平均空间距离缩短至12.3μm(正常组为28.5μm),SBJDD治疗后恢复至21.6μm
● TCGA数据库分析:CCL22表达与 FOXP3、CTLA4 呈显著正相关
● TMA验证:CCL22+ DCs与 CD4+FOXP3+Tregs丰度呈显著正相关
04
临床样本验证SBJDD重塑微环境
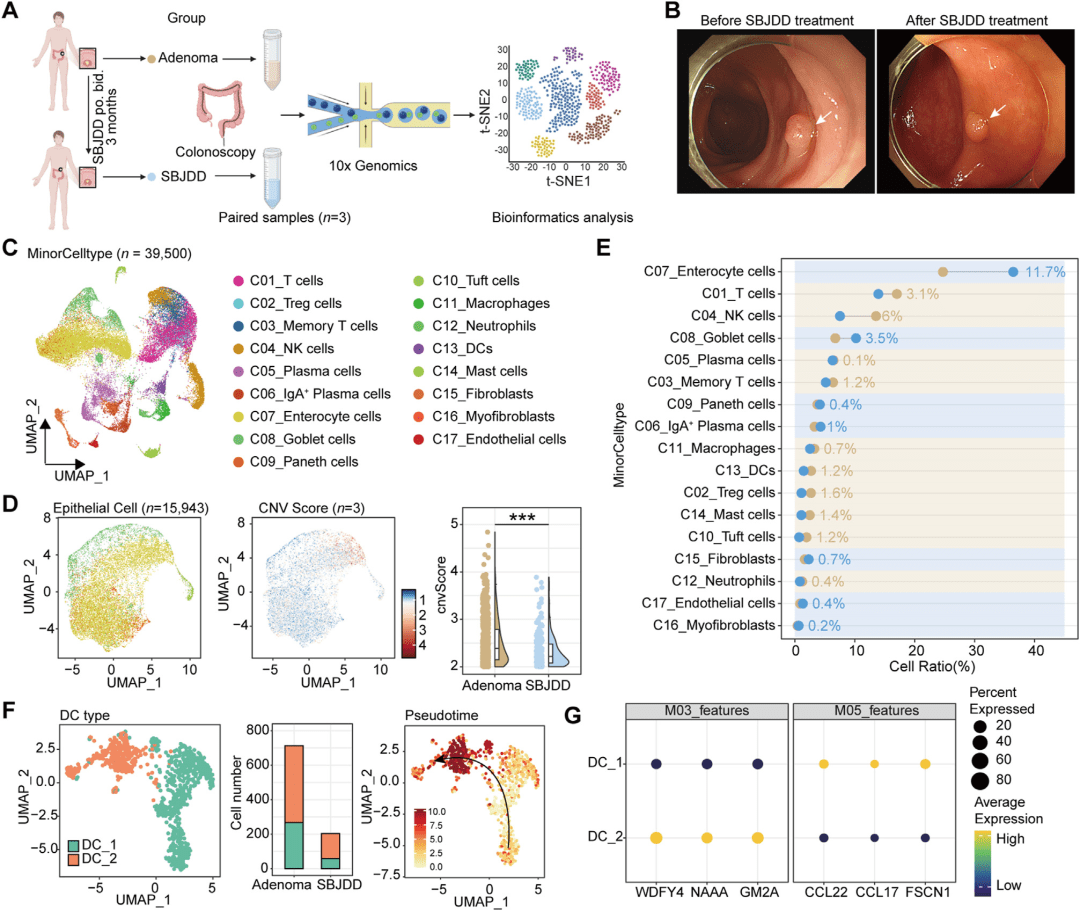
收集3例多发性结直肠腺瘤患者治疗前后的配对组织样本(共6份),进行10x Genomics单细胞RNA测序(总细胞数39,500个)。CNV分析评估上皮细胞恶性程度。拟时序分析追踪DC分化轨迹。
具体发现:
● 治疗后腺瘤体积缩小,CNV评分显著降低
● UMAP聚类显示17个细胞亚型,治疗后DC与Treg细胞比例下降
● DC进一步分为DC_1与DC_2两个亚型,治疗后DC_2比例显著减少
● 拟时序分析显示DC_2来源于DC_1,位于分化轨迹末端,伴随MHC分子表达下调
● 分子特征对比:DC_1与小鼠M03 DCs相似,DC_2与小鼠M05 (Ccl22+) DCs相似
05
Ccl22+DCs的诱导与功能验证
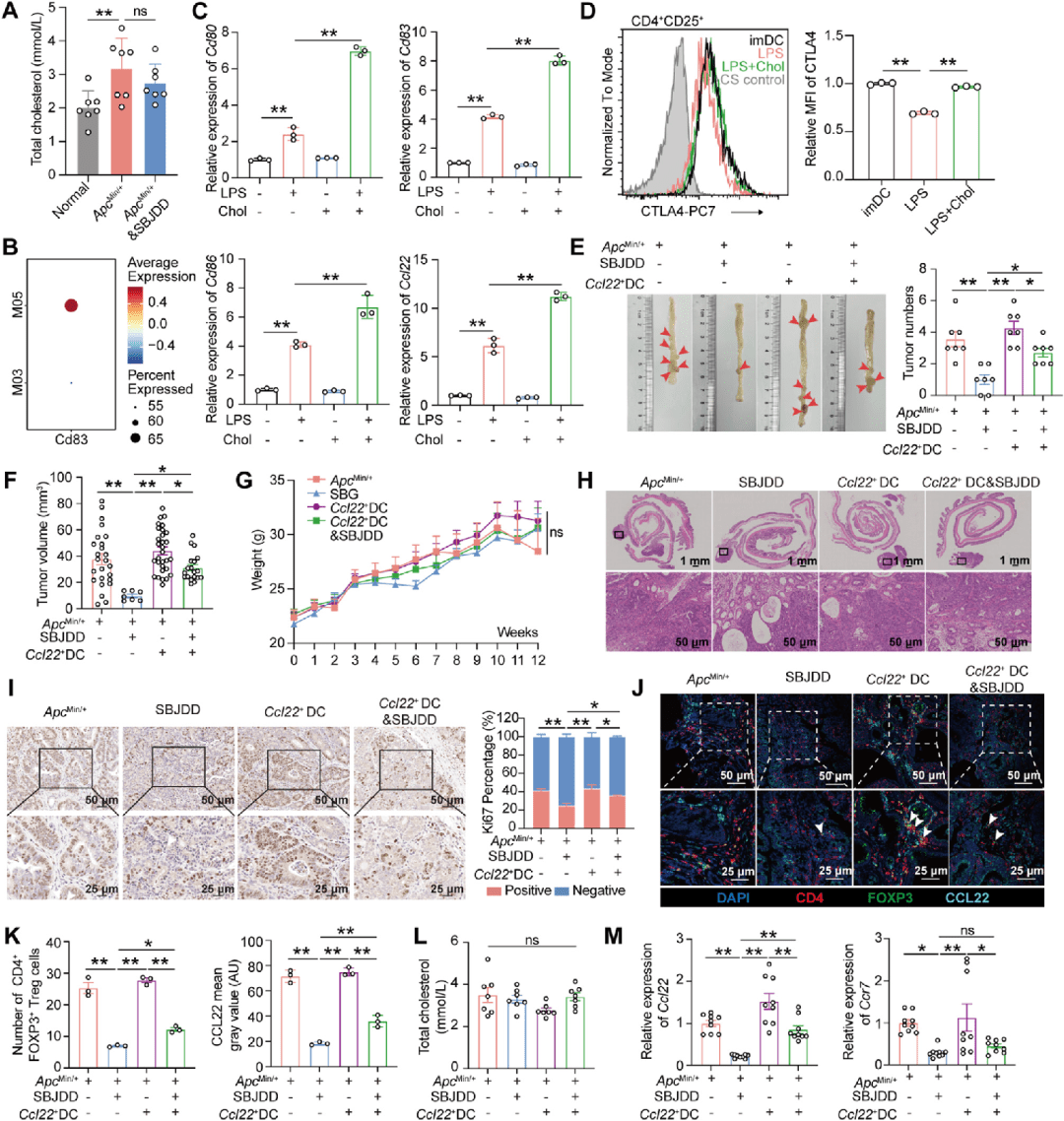
从小鼠骨髓分离imDCs,用LPS(100 ng/mL)联合胆固醇(50 μg/mL)诱导 Ccl22+DCs分化(体外实验,n=3/组)。磁珠分选 CD4+CD62L+ naive T细胞诱导Treg分化。将诱导的 Ccl22+DCs腹腔注射至 ApcMin/+ 小鼠(1×106细胞/只,每周1次),评估肿瘤负荷(n=7/组)。
具体发现:
● 胆固醇联合LPS显著上调 Ccl22、Ccr7、Cd80、Cd86 表达(较单药组增加2-4倍)
● 诱导的 Ccl22+ DCs与Treg共培养后,Treg中CTLA4表达升高(MFI值从342升至587)
● 体内实验:SBJDD单独治疗组肿瘤数降至4.1个,联合 Ccl22+ DCs注射后肿瘤数回升至10.6个(与模型组无显著差异),证实 Ccl22+DCs可逆转SBJDD疗效
● Ki67阳性细胞比例:SBJDD组(18.5%)→ SBJDD+ Ccl22+ DCs组(39.2%)
06
TMEM131通过TNF信号通路调控Ccl22+) DCs
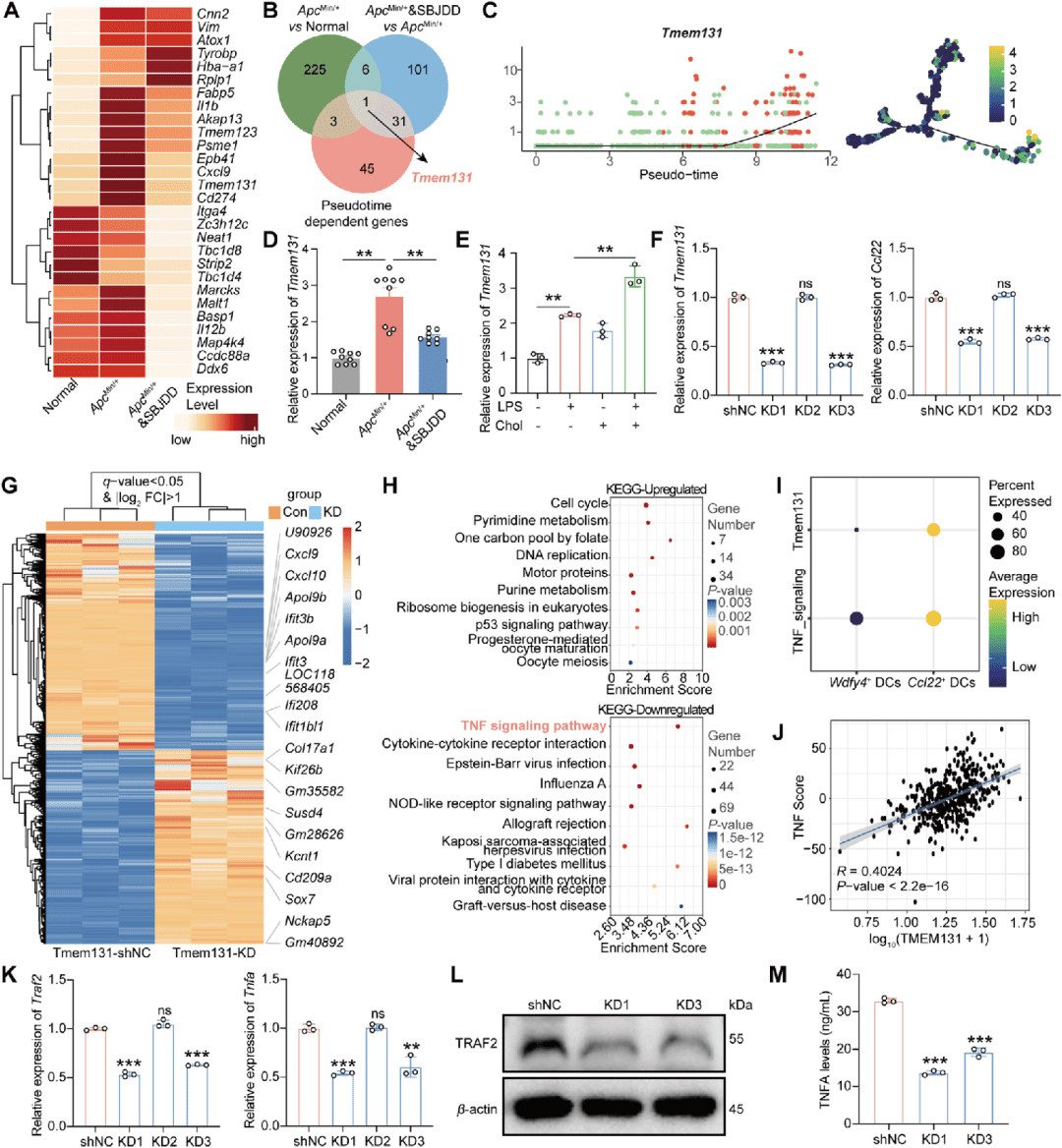
对 Ccl22+ DCs进行差异表达基因分析(不同干预组间)。构建TMEM131 shRNA慢病毒(3条序列)敲低 Ccl22+DCs中TMEM131表达,进行bulk RNA-seq(n=3/组)。qPCR与Western blot验证TNF通路分子。基于TCGA数据库分析 TMEM131 与TNF通路相关性。
具体发现:
● 差异基因与拟时序基因交集筛选出 Tmem131
● 拟时序轨迹显示 Tmem131 在 Ccl22+ DCs分化过程中表达量递增(从Wdfy4⁺ DCs的2.1倍升至末端的6.8倍)
● 敲低TMEM131后,Ccl22表达下降72%,TNF通路分子 Traf2(下降65%)、Tnfa(下降58%)显著下调
● TCGA分析:TMEM131 表达与TNF通路评分呈正相关
● KEGG富集分析显示敲低组下调基因显著富集于TNF信号通路
07
小檗碱是SBJDD中靶向TMEM131的活性成分
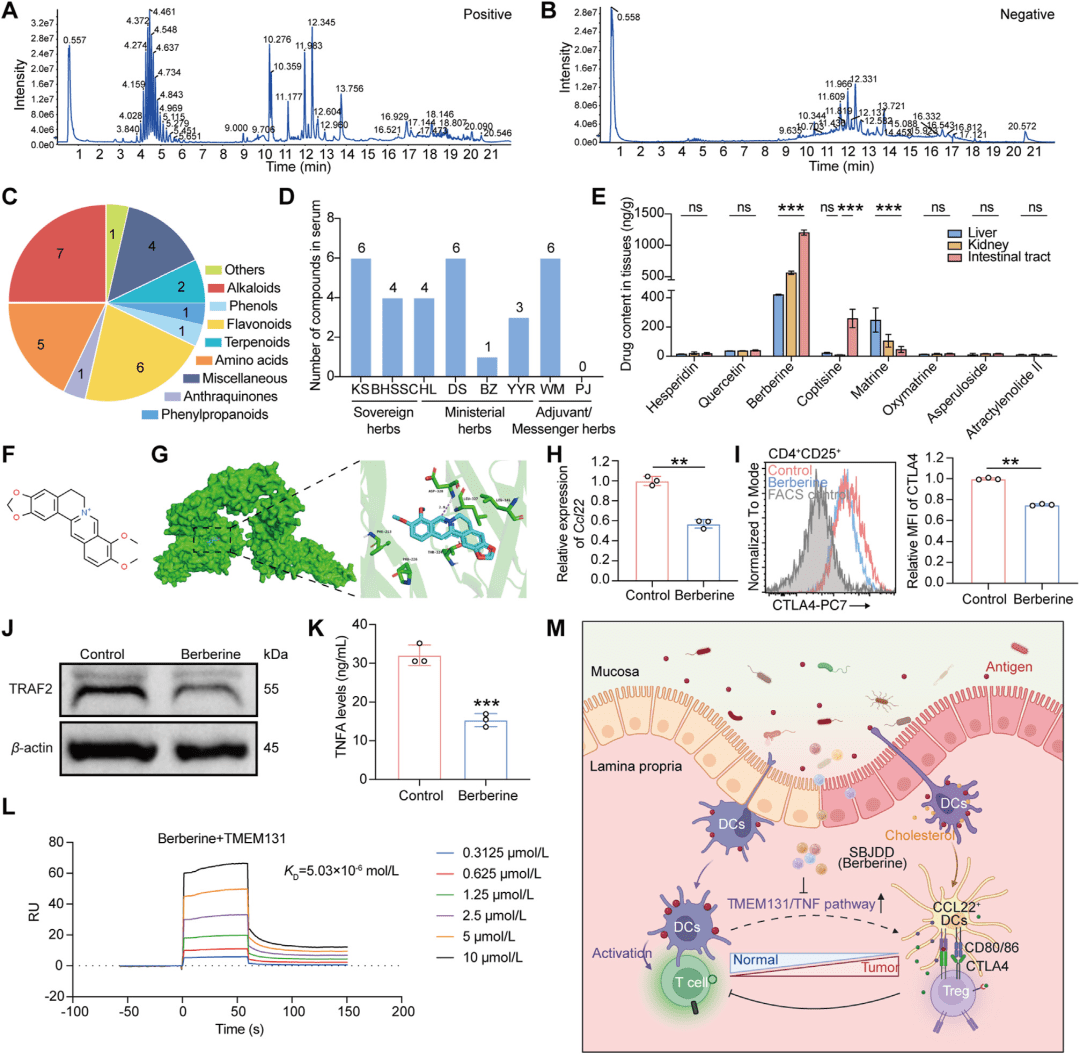
采用UHPLC-QTOF-MS分析SBJDD灌胃后小鼠血清中的入血成分(n=3)。UHPLC-QTRAP-MS/MS定量检测小檗碱含量。分子对接(CB-Dock2)预测小檗碱与TMEM131的结合模式。表面等离子体共振(SPR)测定结合亲和力。体外实验:小檗碱(20 μmol/L)处理 Ccl22+DCs,检测相关基因表达及TNF通路分子。
具体发现:
● 血清中鉴定出28种原型成分,包括7种生物碱、6种黄酮等,小檗碱在肠道组织中显著富集
● 分子对接显示小檗碱与TMEM131结合能为-7.5 kcal/mol
● SPR测定结合常数 KD=5.03×10−6mol/L,证实中等强度直接结合
● 小檗碱处理后,Ccl22+DCs中 Ccl22下降62%、Ccr7下降54%,TRAF2蛋白下降58%、TNFA下降47%
● 小檗碱处理后的 Ccl22+ DCs与Treg共培养,Treg中CTLA4 MFI值从568降至314
总结
本研究通过单细胞转录组学与成分分析相结合的策略,系统阐明了参白解毒方(SBJDD)延缓结直肠肿瘤发生的作用机制:
1. 关键细胞亚群:Ccl22+树突状细胞是一种免疫抑制性DC,在肿瘤微环境中显著富集,与Treg细胞协同形成免疫抑制网络;
2. 核心分子靶点:TMEM131通过调控TNF信号通路,驱动Ccl22+ DCs 的分化与功能;
3. 主要活性成分:小檗碱是SBJDD中靶向TMEM131的关键效应分子,可抑制该通路活化;
4. 治疗意义:SBJDD通过减少 Ccl22+DCs 的浸润与免疫抑制功能,重塑肿瘤微环境稳态,延缓肿瘤发生。
该研究为中药复方“成分-靶点-细胞-通路”的系统性机制解析提供了范例,也为结直肠癌的免疫预防与治疗提供了新的策略与候选分子。
参考文献:
Tao, Yuquan et al. “Single-cell RNA sequencing reveals Shen-Bai-Jie-Du decoction retards colorectal tumorigenesis by regulating the TMEM131-TNF signaling pathway-mediated differentiation of immunosuppressive dendritic cells.” Acta pharmaceutica Sinica. B vol. 15,7 (2025): 3545-3560. doi:10.1016/j.apsb.2025.05.013
